本周看点
1、微芯生物糖尿病1类新药「西格列他钠」即将获批
2、超级抗生素「注射用多黏菌素E甲磺酸钠」迎来首家过评!
3、恒瑞医药环磷酰胺胶囊申报上市并被纳入优先审评公示
4、绿叶制药地舒单抗生物类似药申报上市
本期(10月8日至10月15日),微芯生物糖尿病1类新药「西格列他钠」进入在审批,超级抗生素「注射用多黏菌素E甲磺酸钠」迎来首家过评,第二个地舒单抗生物类似药申报上市,多款新药获批进口,更多动态如下:
国内审评审批·新动态
本周CDE有76个受理号(55个品种)报生产办理状态更新,其中微芯生物西格列他钠、武田富马酸伏诺拉生片、赛诺菲氯吡格雷阿司匹林片、强生达雷妥尤单抗注射液(皮下注射),以及正大天晴的注射用多黏菌素E甲磺酸钠备受关注,更多动态如下:

数据来源:药智数据
微芯生物糖尿病1类新药「西格列他钠」即将获批!
药智数据显示,微芯生物治疗糖尿病的1类新药西格列他钠的新药上市申请已进入“在审批”,有望于近期获批上市。据悉,西格列他钠(Chiglitazar Sodium)是一种全新非TZD结构的PPAR全激动剂,能够平衡且不过度激活PPARα、δ和γ三个受体亚型。
2021年7月,微芯生物发布新闻稿称,Science Bulletin期刊发表了两项确证性3期临床试验结果,这也是全球首个PPAR全激动剂用于治疗2型糖尿病(T2DM)的3期临床试验报道。综合结果表明,患者经西格列他钠治疗24周后,糖化血红蛋白(HbA1c)绝对值较治疗前降低1.32%~1.52%,两个剂量均显示出具有持续和有临床意义的血糖控制作用。在有效控制HbA1c同时,西格列他钠两个剂量组在空腹血糖、胰岛素抵抗指数、餐后2小时血糖、游离脂肪酸、甘油三酯等一系列次要疗效终点指标中,均显示出优于对照药的疗效趋势。
此外,微芯生物于2020年底已宣布与海正药业达成战略合作,将西格列他钠片在中国19个省份区域的推广权独家授予海正药业。
超级抗生素「注射用多黏菌素E甲磺酸钠」,迎首家过评
药智数据显示,正大天晴以注册分类3类递交的“注射用多黏菌素E甲磺酸钠”上市申请已获得批准。该申请曾以“重大专项”被NMPA药品审评中心(CDE)纳入优先审评程序,拟定适应症为:适用于敏感革兰阴性杆菌引起的急性或慢性感染,特别是由铜绿假单胞菌和鲍曼不动杆菌敏感株所致者,亦可用于疑为革兰阴性菌所致严重感染和敏感革兰阴性杆菌感染的初始治疗。
多黏菌素E甲磺酸钠是治疗多重耐药绿脓杆菌等革兰氏阴性菌引起感染的首选药物,而且与其他种类抗生素或抗菌药不会产生交叉耐药性,有望成为治疗耐药菌的一线用药。其原研药最早由Par Sterile Products开发,英文名为Colistimethate Sodium for Injection(商品名:Coly-MycinM),但该产品尚未在中国获批。
截止目前为止,只有正大天晴药业一家企业按照新注册分类批准之后视同通过一致性评价,为该品种首家。但江苏奥赛康的注射用多黏菌素E甲磺酸钠也已进入“在审批”,有望于近期获批上市。
多款新药获批进口
武田富马酸伏诺拉生片获批新适应症
武田旗下创新抑酸药物富马酸伏诺拉生片在中国获批新适应症,用于反复发作的反流性食管炎(Reflux Esophagitis, 简称RE) 患者的维持治疗。此前,该药已获批用于反流性食管炎的初始治疗。
富马酸伏诺拉生片是国内首个获批的钾离子竞争性酸阻滞剂(P-CAB),通过阻断H+,K+-ATP酶的K+通道,竞争性阻滞K+与该酶的结合,可长时间停留于胃壁细胞,从而快速抑制胃酸的分泌,临床数据表明其具有加速黏膜愈合、快速缓解症状的特点。
赛诺菲心血管领域创新药在国内获批
赛诺菲氯吡格雷阿司匹林片获国家药品监督管理局批准上市,用于预防已同时服用氯吡格雷和阿司匹林的急性冠状动脉综合征成年患者的动脉粥样硬化血栓形成事件。
公开资料显示,这是一种抗血小板单片复方制剂(SPC),采用创新"Tab in tab(片中片)"剂型,一日1片,餐前餐后均可服用,使用更为方便,胃肠道不良反应少,有助于提高患者双抗治疗依从性,是适用于双抗的长期给药方式。
杨森CD38单抗国内获批皮下注射新剂型
杨森CD38单抗达雷妥尤单抗注射液(皮下注射)上市申请在中国获得批准,适应症为:治疗原发性轻链型淀粉样变患者。该申请曾被CDE以“临床急需的短缺药品、防治重大传染病和罕见病等疾病的创新药和改良型新药”为由纳入优先审评。
杨森公司的达雷妥尤单抗是国内首个获批的靶向作用于CD38的全人源单克隆抗体。此前已在中国获批静脉注射剂型。达雷妥尤单抗皮下注射剂(英文商品名:Darzalex Faspro)是由达雷妥尤单抗和重组人透明质酸酶PH20(rHuPH20)组成的固定剂量复方。
国内审评审批·新受理
本周CDE新增报生产受理号50个,共36个品种,其中博安生物地舒单抗和恒瑞医药环磷酰胺胶囊备受关注,更多动态见下表:
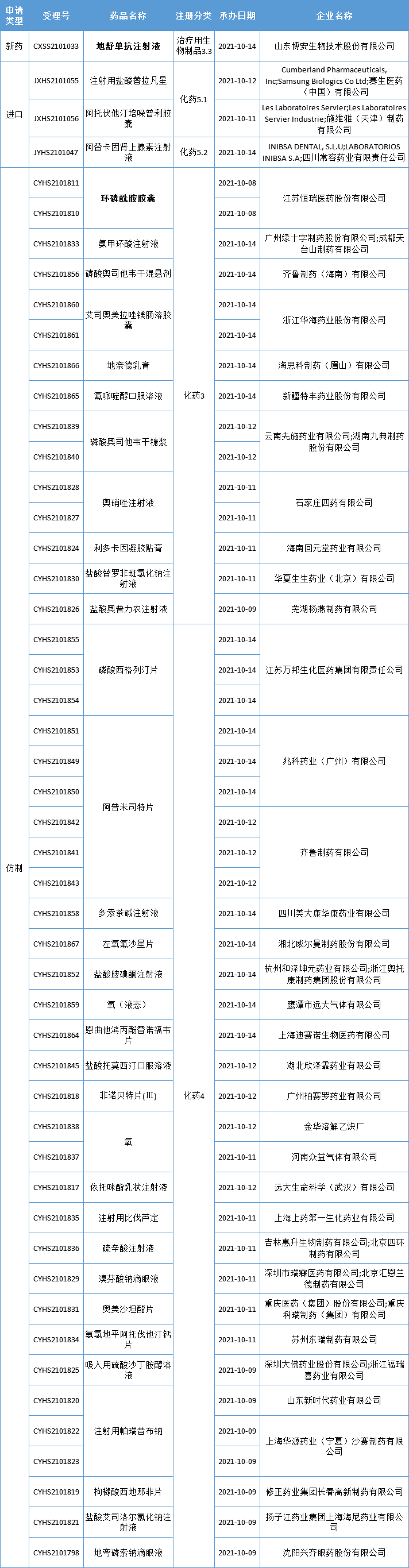
数据来源:药智数据
第二家!绿叶制药地舒单抗生物类似药申报上市
10月14日,绿叶制药集团控股子公司博安生物开发的地舒单抗注射液(LY06006 / BA6101)的上市许可申请获CDE受理。LY06006 / BA6101是IgG2全人源单克隆抗体,为Prolia®的生物类似药。
地舒单抗是一种特异性靶向核因子κB受体活化因子配体(RANK-L)的抗体,由安进公司研发上市。在国内,地舒单抗(安加维®)于 2019 年 5 月获批上市,用于治疗不可手术切除或者手术切除可能导致严重功能障碍的骨巨细胞瘤。2020 年 6 月,其用于骨折高风险的绝经后妇女的骨质疏松症的适应症获 NMPA 批准;同年 11 月,又获批用于多发性骨髓瘤和实体瘤骨转移患者中骨相关事件的预防。目前,安加维“限不可手术切除或手术切除后可能导致严重功能障碍的骨巨细胞瘤”适应症已通过谈判降价 80% 进入医保乙类目录。
药智数据显示,国内首个地舒单抗生物类似药上市申请来自齐鲁制药,博安生物是第二家申报上市的企业。目前国内还有多个处于临床试验阶段,其中康宁杰瑞、上海迈威和博安生物的地舒单抗也已进入3期临床。
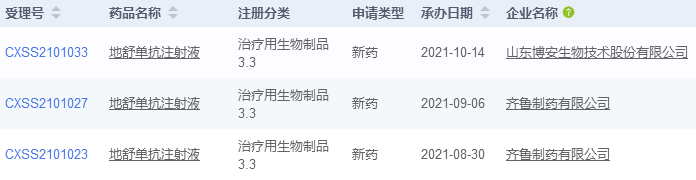
数据来源:药智数据
恒瑞医药环磷酰胺胶囊申报上市并被纳入优先审评公示
近日,恒瑞医药的环磷酰胺胶囊注册申请获国家药品监督管理局受理,且被国家药品监督管理局药品审评中心作为符合儿童生理特征的儿童用药品新品种、剂型和规格纳入拟优先审评品种公示名单,拟定适应症(或功能主治)为:恶性淋巴瘤(Ann Arbor分期 III期和IV期),霍奇金淋巴瘤,淋巴细胞性淋巴瘤(结节性或弥漫性),混合细胞型淋巴瘤,组织细胞性淋巴瘤,伯基特淋巴瘤;多发性骨髓瘤;白血病:慢性淋巴细胞性白血病,慢性粒细胞性白血病(急性原始细胞危象通常无效),急性髓性和单核细胞性白血病,急性淋巴细胞性(干细胞)白血病(缓解期间给予环磷酰胺可有效延长缓解期);蕈样真菌病(晚期);成神经细胞瘤(弥散性疾病);卵巢腺癌;视网膜母细胞瘤;乳腺癌。
环磷酰胺(CTX)是广泛应用的抗癌药物之一。注射用环磷酰胺由Baxter Oncology GmbH公司开发。恒瑞医药注射用环磷酰胺已通过仿制药质量和疗效一致性评价,恒瑞医药成为该品种通过仿制药一致性评价的首家公司。但目前尚未有环磷酰胺胶囊剂型获批上市。
数据来源:药智数据、企业公告等网络公开数据
信息来源:药智网、企业公告等网络公开信息