本周看点
1、2个中药创新药获批上市,2021年已有11个中药新药获批!
2、豪森药业阿美乐获批一线治疗NSCLC
3、再鼎医药抗感染新药「甲苯磺酸奥玛环素」获批上市
4、德琪医药首款新药在中国获批
5、神州细胞阿达木单抗生物类似药报产
本期(12月10日至12月17日),两款中药创新药获批上市,再鼎医药第四款新药获批,豪森药业阿美乐获批一线治疗NSCLC,德琪医药首款新药在中国获批,恒瑞、君实PD-1新适应症不断增加,国产第7款阿达木单抗生物类似药报产,更多动态如下:
国内审评审批·新动态
本周CDE有75个受理号(54个品种)报生产办理状态更新,其中再鼎医药的ZL-2401对甲苯磺酸盐片和注射用ZL-2401对甲苯磺酸盐,豪森药业的甲磺酸阿美替尼片,以岭药业的苏夏解郁除烦胶囊和一力制药的虎贞清风胶囊,以及德琪医药的ATG-010片备受关注。更多动态如下:
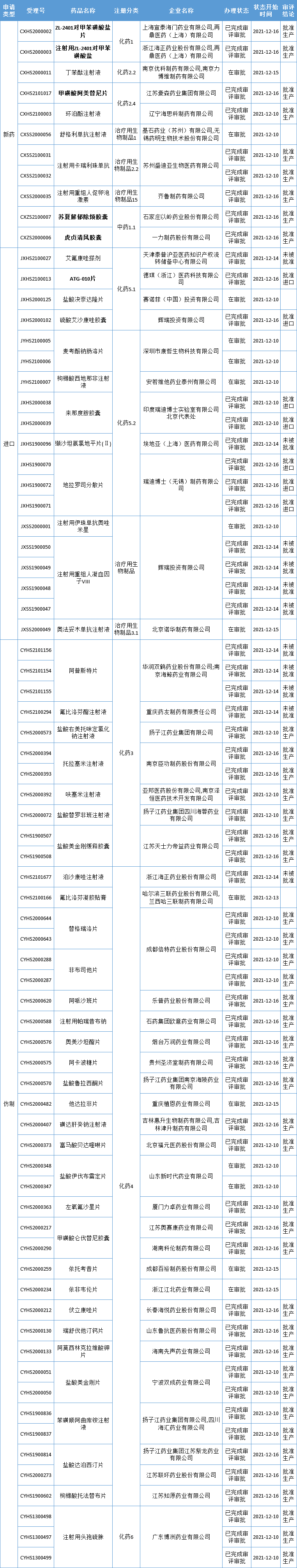
数据来源:药智数据
中药创新药虎贞清风胶囊、解郁除烦胶囊获批上市!
本周又有两款中药创新药获批上市,包括虎贞清风胶囊和解郁除烦胶囊。
虎贞清风胶囊,是在临床经验方基础上研制的中药创新药,开展了随机、双盲、安慰剂平行对照、多中心临床试验,临床试验研究结果显示可用于轻中度急性痛风性关节炎中医辨证属湿热蕴结证的治疗。药品上市许可持有人为一力制药股份有限公司。
解郁除烦胶囊,是在临床经验方基础上研制的中药创新药,处方根据中医经典著作《金匮要略》记载的半夏厚朴汤和《伤寒论》记载的栀子厚朴汤化裁而来,开展了随机、双盲、阳性对照药(化学药品)、安慰剂平行对照、多中心临床试验,临床试验研究结果显示可用于轻中度抑郁症中医辨证属气郁痰阻、郁火内扰证的治疗。药品上市许可持有人为石家庄以岭药业股份有限公司。
药智数据统计,2021年已有11个中药新药获批,包括:虎贞清风胶囊、解郁除烦胶囊、玄七健骨片、芪蛭益肾胶囊和坤心宁颗粒、银翘清热片、益气通窍丸、益肾养心安神片,以及国家药品监督管理局通过特别审批程序应急批准的清肺排毒颗粒、化湿败毒颗粒、宣肺败毒颗粒。
再鼎医药抗感染新药「甲苯磺酸奥玛环素」获批上市
近日,再鼎医药纽再乐®(ZL-2401,甲苯磺酸奥马环素)的新药上市申请获得国家药监局批准,用于治疗社区获得性细菌性肺炎(CABP)及急性细菌性皮肤和皮肤结构感染(ABSSSI)。这是再鼎医药获批的第四款产品,也是其在抗感染疾病领域获批的首款产品。
甲苯磺酸奥玛环素是一款每日一次的、拥有口服和静脉输注两种剂型的新型四环素类抗菌药,专门设计用于克服四环素类耐药性并提高广谱抗菌活性,如革兰阳性、革兰阴性、非典型和许多其他病原体引起的感染。2018年10月,美国FDA已批准这款创新抗生素上市,用于治疗CABP和ABSSSI的成人患者。
2017年4月,再鼎医药从Paratek公司获得该药物在中国大陆、香港、澳门和台湾地区开发、生产和推广的独家许可。2020年,再鼎医药将纽再乐在中国内地的独家推广权授予瀚晖制药有限公司全资子公司—辉正(上海)医药科技有限公司。
豪森药业阿美乐获批一线 治疗NSCLC
药智数据显示,豪森药业的1类创新药阿美乐®(甲磺酸阿美替尼片)新适应症获得批准,用于具有表皮生长因子受体(EGFR)外显子19缺失或外显子21(L858R)置换突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗。这是阿美乐®获批的第二个适应症。
甲磺酸阿美替尼片是豪森药业自主研发的1类创新药,是全球范围内第二款获批的第三代 EGFR 抑制剂,也是首个中国原创三代 EGFR-TKI。
2020年3月,阿美乐®首个适应症获批上市,用于治疗既往经EGFR-TKI治疗进展,且T790M突变阳性的局部晚期或转移性NSCLC患者;在同年 12 月的医保谈判中,阿美替尼谈判成功进入医保乙类。2021年5月,阿美替尼的新适应症上市申请被CDE纳入优先审评,并获国家“重大新药创制”科技重大专项立项支持。
此前国内三代 EGFR 中仅阿斯利康的奥希替尼获批一线适应症,本次阿美替尼一线适应症获批为国产首家。此外在 12 月初,艾力斯的伏美替尼也申报了这一适应症。
此外,豪森还在进行阿美乐®联合含铂双药化疗一线治疗有敏感突变NSCLC、辅助治疗NSCLC等适应症的多个临床研究。2020年7月,豪森药业宣布授予EQRx公司排他性许可,在中国境外开发、生产和商业化其阿美替尼。
德琪医药首款新药塞利尼索在中国获批!
德琪医药塞利尼索(ATG-010)(商品名:希维奥)获得国家药监局的附条件上市批准,适用于与地塞米松联用,既往接受过治疗且对至少一种蛋白酶体抑制剂,一种免疫调节剂以及一种抗CD38单抗难治的复发或难治性多发性骨髓瘤成人患者的治疗。这是德琪医药成立以来在中国获批的首款新药。
据悉,塞利尼索是目前首款且唯一一款被美国FDA批准的口服XPO1抑制剂,也是首款可用于治疗多发性骨髓瘤和弥漫性大B细胞淋巴瘤的药物。
德琪医药通过与Karyopharm的独家授权协议获得了三款SINE药物在多个亚太市场的开发和商业化权益,包括ATG-010(塞利尼索)、ATG-016(eltanexor)和ATG-527(verdinexor)。
今年7月底,塞利尼索已在韩国通过优先评审程序获得了塞利尼索的上市许可。2021年初,塞利尼索在中国递交新药上市申请,并在2月份被纳入优先审评。8月,德琪医药与上药控股就塞利尼索在中国的进口授权、分销业务、供应链服务和创新增值等多个层面达成合作。其中,上药控股将作为德琪医药的塞利尼索中国进口总经销。
国内审评审批·新受理
本周CDE新增报生产受理号50个,共32个品种,其中恒瑞医药的注射用卡瑞利珠单抗和神州细胞的阿达木单抗注射液备受关注,更多动态见下表:
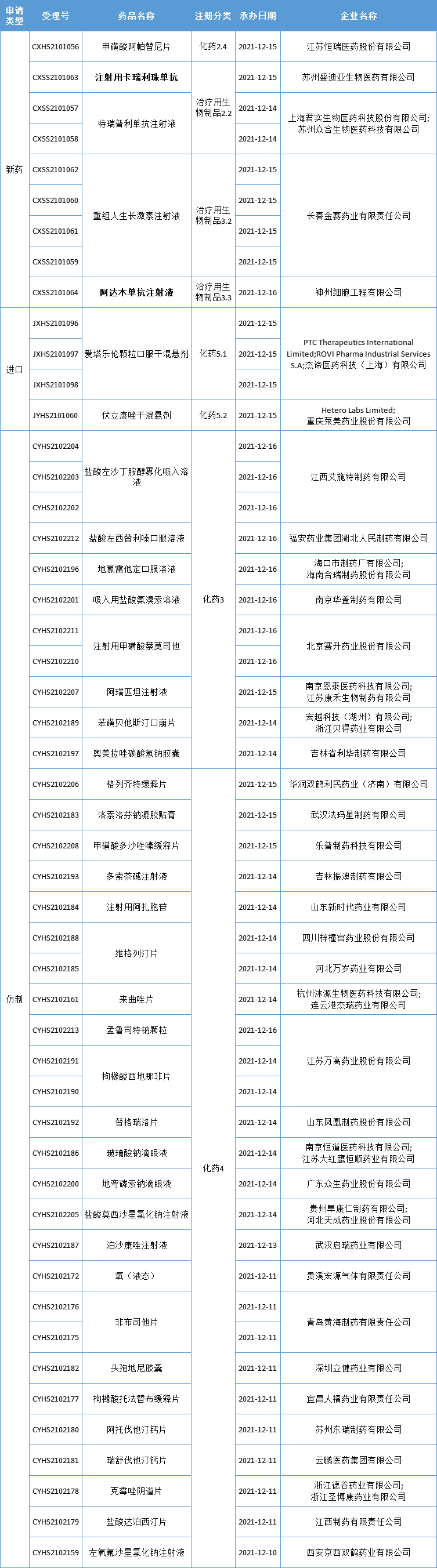
数据来源:药智数据
恒瑞卡瑞利珠单抗第9项适应症申报上市
药智数据显示,恒瑞医药的PD-1单抗卡瑞利珠单抗的第9项适应症上市申请已获CDE受理。
注射用卡瑞利珠单抗是恒瑞医药自主研发的人源化抗PD-1单克隆抗体,自2019年5月上市以来,该产品已先后获批8项适应症,包括:
1.三线治疗经典型霍奇金淋巴瘤
2.二线治疗晚期肝细胞癌
3.单药二线治疗晚期食管鳞癌
4.联合培美曲塞和卡铂一线治疗晚期或转移性非鳞癌非小细胞肺癌
5.三线治疗复发/转移性鼻咽癌
6.联合顺铂和吉西他滨一线治疗鼻咽癌
7.联合紫杉醇和顺铂一线治疗食管癌
8.联合化疗一线治疗鳞状非小细胞肺癌(NSCLC)
其中前四项适应症已纳入医保。
此外,恒瑞开发的第二代PD-1抗体也已进入临床。12月8日,恒瑞医药皮下注射PD-1抗体SHR-1901在药物临床试验登记与信息公示平台网站登记了一项1期临床试验,旨在评估SHR-1901在晚期恶性肿瘤受试者中的安全性。
国产第7家:神州细胞阿达木单抗申报上市
药智数据显示,北京神州细胞提交的阿达木单抗注射液(SCT630)生物类似药的上市申请已获CDE受理,拟用于治疗银屑病、 类风湿关节炎及强直性脊柱炎等免疫系统疾病。
阿达木单抗(修美乐)原研由艾伯维开发,是全球首个获批上市的全人源抗肿瘤坏死因子ɑ(TNF-ɑ)单克隆抗体,在美国和欧盟等地区自2002年先后获批治疗类风湿关节炎、强直性脊柱炎、银屑病、银屑病关节炎、幼年特发性关节炎、克罗恩病等多个适应症。原研修美乐已连续8年蝉联全球“药王”,2020年达到销售额峰值198.32亿美元,今年预计将超过200亿美元。
在中国,修美乐最早于2011年获批上市,2019年被纳入国家医保乙类目录。
据药智数据统计,除原研外,国内已有7家企业的阿达木单抗申报上市,包括百奥泰、海正药业、信达生物、复宏汉霖、君实生物、正大天晴和神州细胞,其中前4款已经获批上市,另有多款处于注册申请或临床试验阶段。
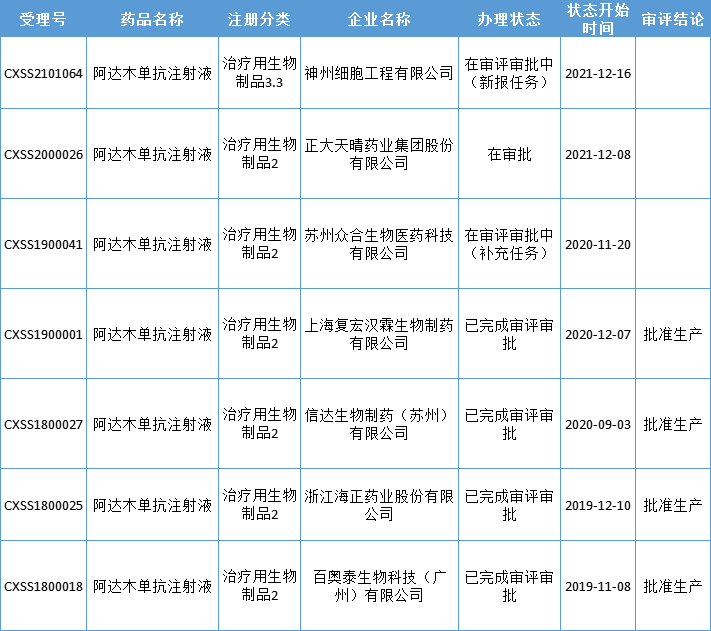
数据来源:药智数据
近日,国内生物类似药密集上市,众多竞品陆续进入商业化阶段,竞争激烈。
数据来源:药智数据、企业公告等网络公开数据
信息来源:药智网、企业公告等网络公开信息