看点:
7月药审中心受理总量为1145个(不计复审)
7月37个国产化药1类新药品种获CDE受理
7月新增73个按仿制药质量和疗效一致性评价申报的受理号
恒瑞医药、百时美施贵宝公司1类新药上市获受理
根据药智数据最新统计,2022年7月份CDE共承办新的药品注册申请以受理号计有1145个(复审除外,下同)其中化药受理834个,中药受理150个,生物制品受理161个;2022年3-7月各类药品注册申请受理情况详见图一。
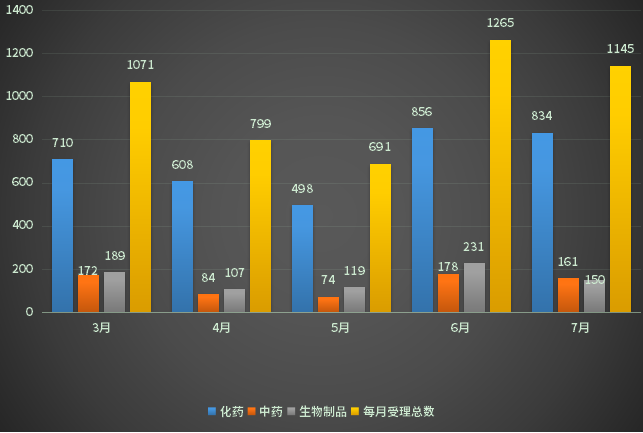
图一 2022年3-7月CDE药品受理情况
数据来源:药智数据、药智咨询整理
以下且看化药、中药、生物制品的注册受理及审评情况详细分析。
一、化药审评情况
7月份CDE承办新的化药注册申请834个(以受理号计),其中新药申请受理号93个,进口受理号81个(其中包括一次性进口15个),仿制申请受理号197个;
以审评任务类别统计,IND申请140个,ANDA申请202个,NDA申请12个,进口再注册申请39个;2022年2-7月CDE化药各审评任务类别申请受理情况详见图二。
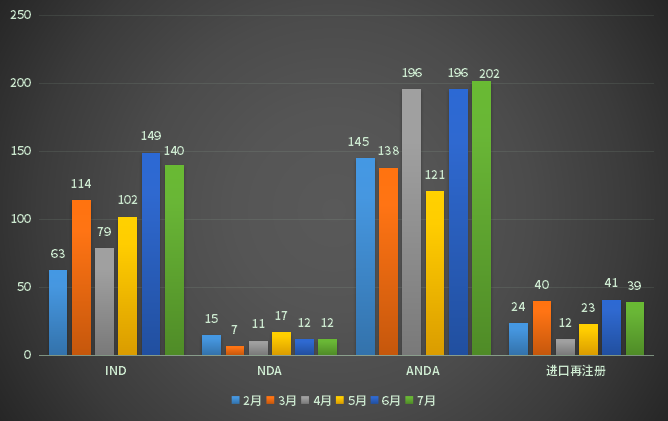
图二 2022年2-7月CDE化药各审评任务类别申请受理情况
数据来源:药智数据、药智咨询整理
1.化药1类国产申报情况
7月CDE受理化药国产1类新药共计77个(按受理号计),其中NDA申请2个,IND申请77个,涉及37个品种(按药品+企业维度统计);下表为7月新承办的1类国产新药。
表一 2022年7月新承办的化药1类国产新药
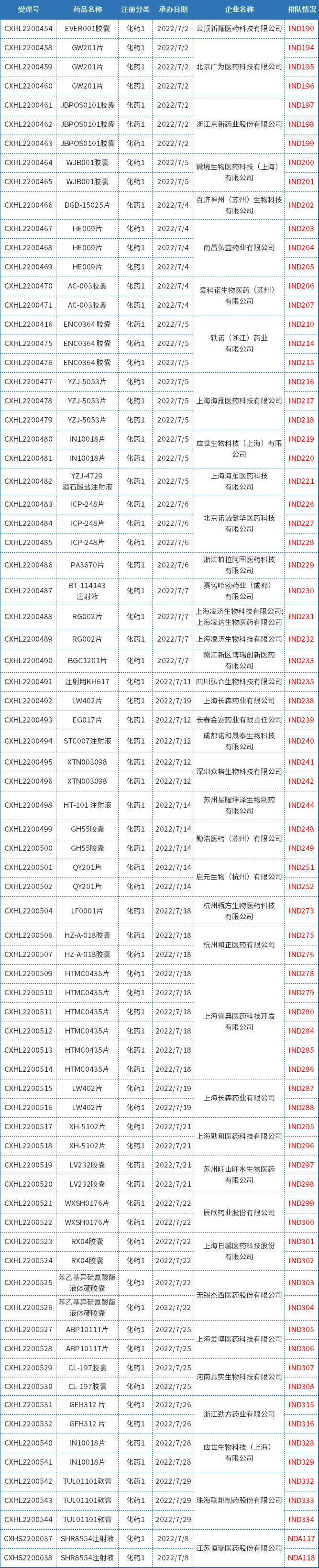
注:排队序号截止至2022年08月02日。
2.化药1类进口药品申报情况
7月共33个进口化药1类受理号获得承办,其中NDA申请1个,IND申请32个,共15个品种,目前,均已进入相应序列排队待审;下表为7月新承办的1类进口新药。
表二 2022年7月新承办的化药1类进口新药
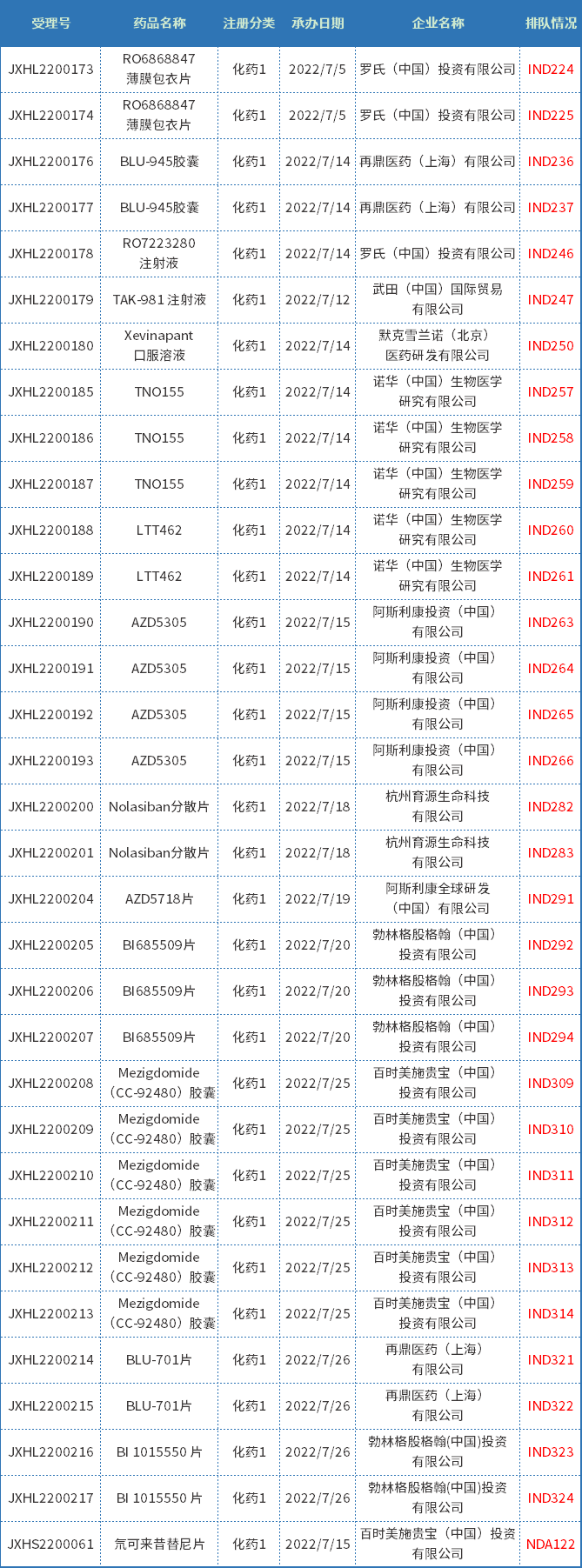
注:排队序号截止至2022年08月02日
JBPOS0101胶囊
JBPOS0101胶囊是韩国B-PS公司开发的一款在研新药,它通过结合代谢型谷氨酸受体减少神经元放电,进而控制癫痫发作;2021年8月26日,京新药业宣布与韩国B-PS公司达成合作,获得癫痫1类新药JBPOS0101在中国地区的独家权益。目前京新药业递交该药在国内临床申请已获得受理。
HE009片
HE009片是南昌弘益药业有限公司自主研发、拥有自主知识产权的S1P1小分子抑制剂调节剂,拟用于系统性红斑狼疮(SLE)的治疗。
ICP-248片
ICP-248片是诺诚健华自主研发的1类创新药,是一种新型的高选择性BCL2抑制剂,拟用于单药或与BTK抑制剂等其他药物联合治疗非霍奇金淋巴瘤(NHL)、急性淋巴细胞白血病 (ALL)等恶性血液系统肿瘤。
BT-114143注射液
BT-114143是赛诺哈勃自主研发的一款全新小分子纤维蛋白溶解酶/酶原(Plasminogen)抑制剂,拟用于治疗和预防纤维蛋白溶解亢进引起的各种出血和疾病。
SHR8554注射液
SHR8554注射液是恒瑞医药自主研发的1类新药,是一种靶向μ阿片受体(MOR)的小分子药物,可激活MOR受体,适用于术后镇痛治疗。目前该药品上市上市申请已获受理。
氘可来昔替尼片
氘可来昔替尼片是百时美施贵宝公司(BMS)开发的一种口服、选择性酪氨酸激酶2(TYK2)别构抑制剂,具有独特的作用机制。它通过与TYK2的调节结构域结合,实现高度选择性。
3.化药改良型新药申报情况
7月新增化药2类改良型新药30个(按受理号计),其中IND申请27个,NDA申请3个,共涉及18个品种;2022年2-7月CDE化药改良型新药申请受理情况详见图三。
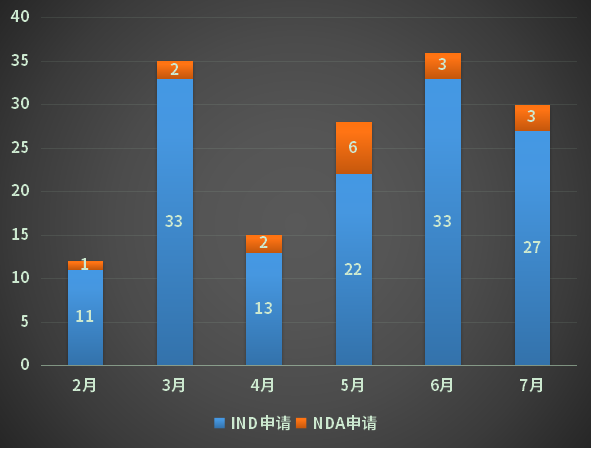
图三 2022年2-7月CDE化药改良型新药申请受理情况
数据来源:药智数据、药智咨询整理
二、中药审评情况
7月份CDE承办的中药注册申请受理号共计150个,其中新药5个,补充申请67个;2022年2-7月CDE中药各申请类型受理情况详见图四。
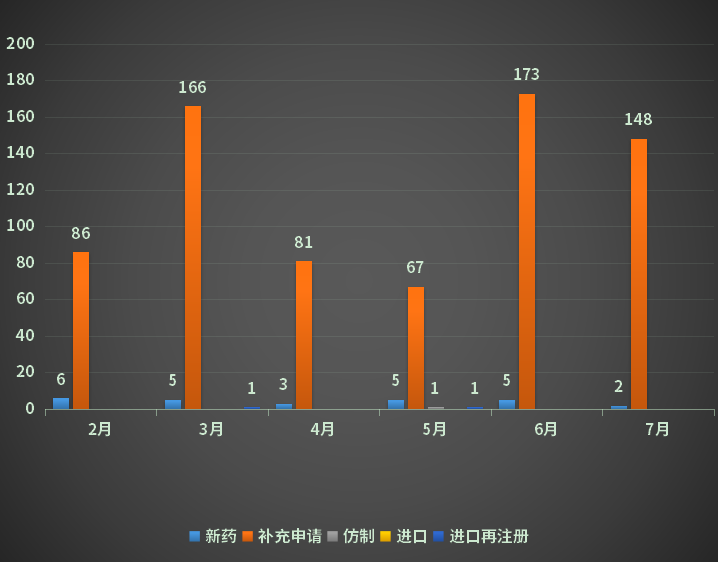
图四 2022年2-5月CDE中药各申请类型受理情况
数据来源:药智数据、药智咨询整理
1.中药1类新药申报情况
7月共承办2个中药1类创新药,均是IND申请;下表为7月新承办的中药新药。
表三 2022年7月新承办的中药新药

注:排队序号截止至2022年08月02日
三、生物制品审评情况
7月份CDE承办新的生物制品注册申请受理号共计161个,新药48个,补充申请57个,进口50个(其中包括一次性进口8个),进口再注册6个;2022年27月CDE生物制品各申请类型受理情况详见图五。
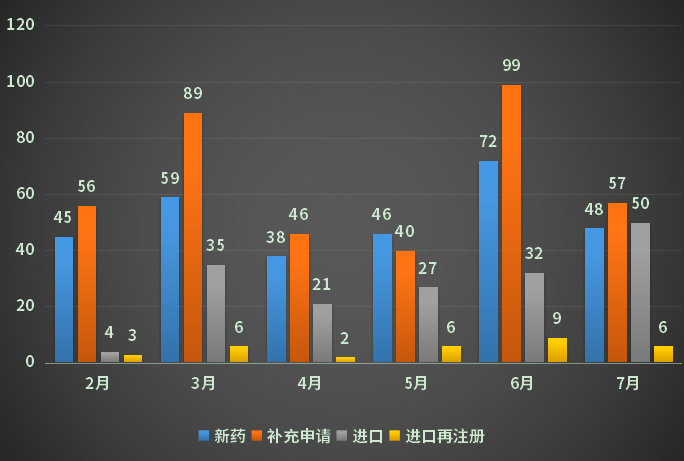
图五 2022年2-7月CDE生物制品各申请类型受理情况
数据来源:药智数据、药智咨询整理
1.生物制品1类新药申报情况
7月有47个1类治疗用生物制品和1个治疗用生物制品受理号获得承办,均是临床试验申请,目前都已经进入相应序列排队待审;下表为7月新承办的治疗用生物制品1类创新药。
表四 2022年7月新承办的治疗用生物制品1类新药
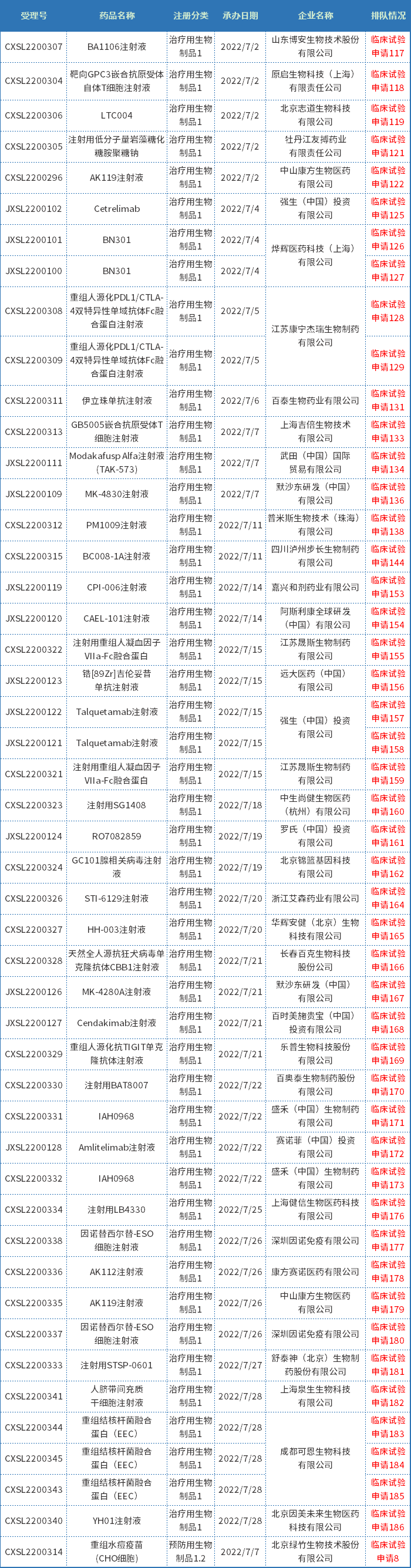
注:排队序号截止至2022年08月02日。
四、按一致性评价申报品种情况
7月新增73个按一致性评价要求进行申报的受理号和233个视同受理号。(篇幅限制仅展示一致性信息,视同及具体信息请关注药智企业版药品注册与受理数据库);2022年2-7月一致性评价受理数量详见图六;表五为7月新增一致性评价受理号信息。
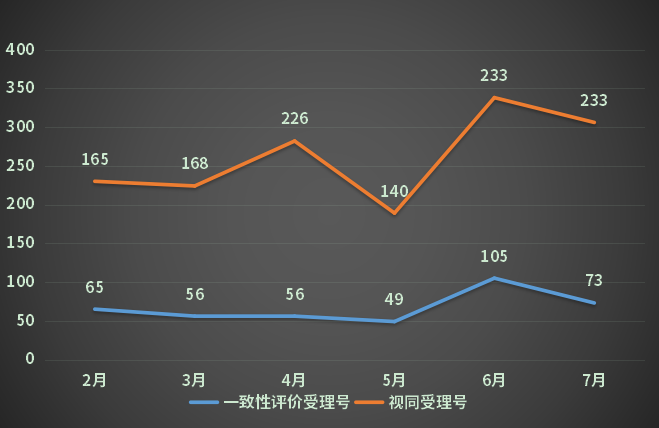
图六 2022年2-7月一致性评价受理数量
数据来源:药智数据、药智咨询整理
表五 2022年7月新增一致性评价受理数据
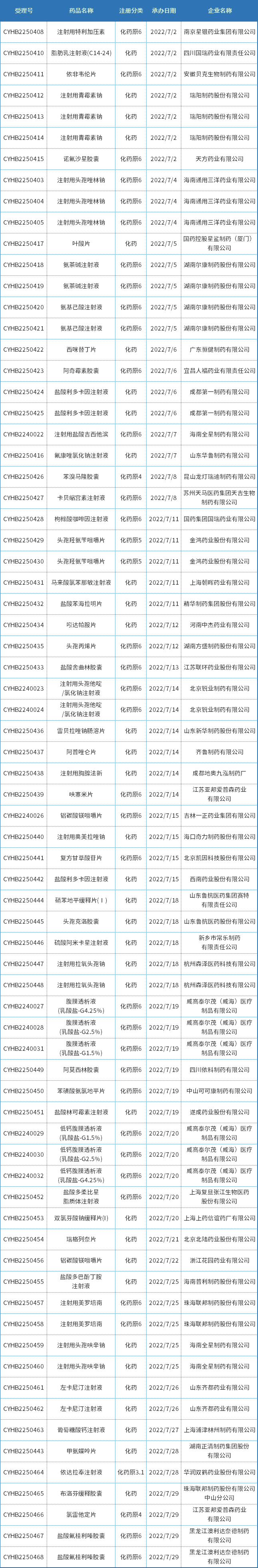
注:排队序号截止至2022年08月02日。
数据来源:药智药品注册与受理数据库