看点:
1、54项新药申请获得临床试验默认许可,包括25款1类新药
2、CDE新受理32个新药(61个受理号)的临床试验申请
3、百济神州3款抗肿瘤单抗获批临床
药智数据显示,本期(10月14日至10月21日)有54项新药申请获得临床试验默认许可,涉及27款国产新药,9款进口新药;另有32个品种(61个受理号)临床申请获CDE承办受理,更多动态如下:
新药临床申请·新获批
本期,54项新药申请获得临床试验默认许可,涉及27款国产新药,9款进口新药。获批临床的创新药涉及BCL-2抑制剂、三代BTK抑制剂、FAK抑制剂、JAK1抑制剂、GARP单抗、LAG-3单抗、OX40激动剂、BTLA单抗、PD-L1/TGF-βRII双功能融合蛋白、HER2 ADC等,适应症涵盖多种血液肿瘤、实体瘤、阿尔茨海默病、炎症性关节病、骨坏死、精神分裂、干眼病等。
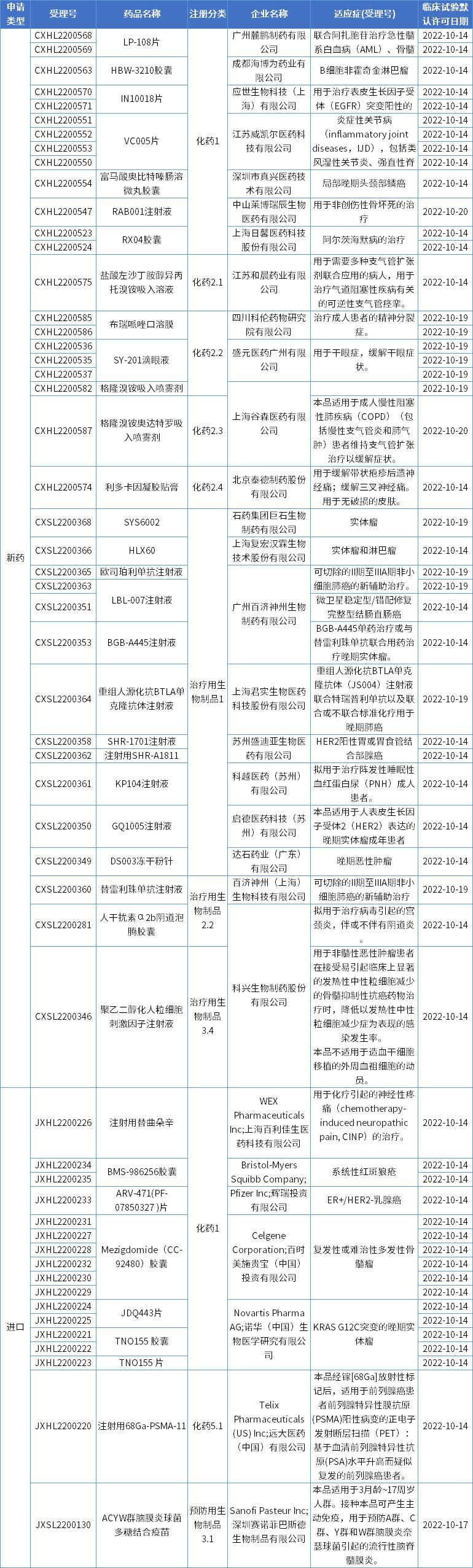
数据来源:药智数据
1.LP-108片
LP-108片是麓鹏制药开发的一种新型、高选择性BCL-2抑制剂,本次获批临床适应症为联合阿扎胞苷治疗急性髓系白血病(AML)、骨髓增生异常综合征(MDS)或慢性粒-单核细胞白血病(CMML)
2.HBW-3210胶囊
HBW-3210胶囊是海博为药业自主研发的强透脑、可逆抗耐药三代BTK抑制剂,拟开发治疗B细胞非霍奇金淋巴瘤。据海博为药业新闻稿,HBW-3210能够克服第一、二代BTK抑制剂由于C481S突变产生的耐药性问题,对野生型和突变型BTK均有很高的抑制活性;且该药具有强透脑性,HBW-3210在透脑性(大鼠透脑率>60% VS ~10%)、有效性等关键成药性方面有着较突出的优势。
3.IN10018片
N10018是应世生物从勃林格殷格翰(BI)引进的一款高效和高选择性的ATP竞争性黏着斑激酶(FAK)抑制剂,目前正在开发用于包括卵巢癌、黑色素瘤、三阴性乳腺癌、头颈部肿瘤、KRAS G12C突变肿瘤、胰腺癌等多种实体瘤适应症。
2020年5月,应世生物与康宁杰瑞达成合作,共同开展PD-L1/CTLA-4双特异性抗体KN046与IN10018组合疗法的临床研究。本次获批的即是IN10018联合KN046以及标准化疗(白蛋白紫杉醇 + 吉西他滨)用于晚期胰腺癌的治疗。
4.VC005片
VC005片是威凯尔医药自主研发的新型、高选择性JAK1抑制剂,能同时有效抑制TYK2等炎症靶点,抑制免疫细胞介导的细胞毒性和免疫应答,对JAK2、JAK3抑制活性较弱,化合物选择性好。该药此前已获批开展炎症性肠病(IBD)临床试验,本次获批适应症为炎症性关节病(inflammatory joint diseases,IJD),包括类风湿性关节炎、强直性脊柱炎等。
5.富马酸奥比特嗪肠溶微丸胶囊
富马酸奥比特嗪肠溶微丸胶囊(SM-1)是深圳市真兴医药研发的潜在“first-in-class”Procaspase-3靶点抗肿瘤药物,目前单药治疗晚期实体瘤研究已进入II期临床,研究结果显示,药物具有良好的安全性和有效性。本次获批的是SM-1联合放疗在局部晚期头颈部鳞状细胞癌受试者中的安全性、药代动力学 I 期临床研究。
6.RAB001注射液
RAB001是中山莱博瑞辰从美国骨和关节再生医学公司(Regenerative Arthritis & Bone Medicine, Inc.)引进的一款针对非创伤性骨坏死的小分子多肽偶联双重靶向创新药。相对于其他外源性干细胞治疗方法,RAB001通过增进内源性干细胞靶向到骨头,改善血液循环,修复骨坏死,刺激新骨形成。
7.RX04胶囊
RX04胶囊是日馨医药开发的一款创新药,拟开展治疗阿尔兹海默症的研究。
8.SYS6002
SYS6002是石药集团巨石生物开发的一款生物1类创新药,拟开展治疗实体瘤的研究。
9.HLX60
HLX60(即重组抗GARP人源化单克隆抗体注射液)是复星医药自主研发的创新型抗GARP单抗,获批开展实体瘤和淋巴瘤的Ⅰ期临床试验。值得一提的是,2022年8月,HLX60联合汉斯状(斯鲁利单抗注射液)用于晚期/转移性实体瘤治疗的Ⅰ期临床试验于澳大利亚获批开展。目前,全球范围内尚无靶向GARP的单克隆抗体获批上市。
10.欧司珀利单抗注射液
欧司珀利单抗(BGB-A1217)是百济神州开发的一款具有完善Fc功能的在研抗TIGIT单克隆抗体,目前已在全球启动多项后期临床试验,本次获NMPA批准的是用于可切除的II期至IIIA期非小细胞肺癌的新辅助治疗。此外,百济神州曾与诺华公司达成战略选择权、合作和授权协议,双方将在北美、欧洲和日本共同开发、生产和商业化欧司珀利单抗。
11.LBL-007注射液
LBL-007注射液是南京维立志博自主研发的一款全人源抗LAG-3抗体药,2021年12月,维立志博授予百济神州LBL-007的全球研发和生产许可,以及中国境外的独家商业化权利。本次获批两项临床试验:可切除的II期至IIIA期非小细胞肺癌的新辅助治疗和微卫星稳定型/错配修复完整型结肠直肠癌
12.BGB-A445注射液
BGB-A445是百济神州开发的一款OX40激动剂抗体,全球范围内尚无同靶点药物上市,阿斯利康、辉瑞、GSK、罗氏等跨国药企的OX40抗体均已进入II期临床阶段,不过罗氏pogalizumab治疗尿路上皮癌的II期临床已终止,原因是患者招募缓慢。此前,BGB-A445已在国外获批临床,本次获NMPA批准在国内开展BGB-A445单药治疗或与替雷利珠单抗联合用药治疗晚期实体瘤临床研究。
13.重组人源化抗BTLA单克隆抗体注射液
icatolimab(TAB004/JS004)是君实生物自主研发的一款特异性针对B和T淋巴细胞衰减因子(BTLA)的重组人源化抗BTLA单克隆抗体。icatolimab于2019年和2020年分别在美国和中国获批进入临床研究,是全球首款进入临床研究的抗肿瘤BTLA(B/T淋巴细胞弱化因子)单抗,目前已进入中美两地Ib/II期临床研究阶段。在今年ASCO年会上,君实生物表示Icatolimab单药或联合特瑞普利单抗治疗R/R淋巴瘤患者都具有良好的耐受性,并表现出初步临床疗效。本次一项新适应症获批临床:JS004联合特瑞普利单抗以及联合或不联合标准化疗用于晚期肺癌。
14.SHR-1701注射液
SHR-1701是恒瑞医药自主研发并具有知识产权的抗PD-L1/TGF-βRII双功能融合蛋白,可以促进效应性T细胞的活化,同时还可有效改善肿瘤微环境中的免疫调节作用,最终有效促进免疫系统对于肿瘤细胞的杀伤。目前,SHR-1701注射液已在中国开展多项实体瘤临床试验,包鼻咽癌、宫颈癌、非鳞非小细胞肺癌、晚期结直肠癌等,并在澳洲开展I期临床试验。本次获批开展HER2阳性胃或胃食管结合部腺癌临床研究。
15.注射用SHR-A1811
注射用SHR-A1811是恒瑞医药自主研发的以HER2为靶点的抗体偶联药物(ADC),此前已获批开展HER2异常非小细胞肺癌、HER2阳性乳腺癌等临床试验,本次获批开展HER2阳性胃或胃食管结合部腺癌临床试验。
16.KP104注射液
KP104是科越医药开发的一款双靶点补体生物制剂。目前,KP104正进入针对多个适应症的2期临床试验,包括IgA肾病(IgAN)、C3肾小球病(C3G)、继发于系统性红斑狼疮的血栓性微血管病(SLE-TMA)和阵发性睡眠性血红蛋白尿症,还曾获得美国FDA授予治疗PNH的孤儿药资格。本次在中国获批的是一项2期临床试验,旨在中国阵发性睡眠性血红蛋白尿症患者中评估KP104的有效性、安全性、耐受性、药代动力学(PK)和药效学(PD)。
17.GQ1005注射液
GQ1005注射液是启德医药开发的一款HER2 ADC药物,拟开展人表皮生长因子受体2(HER2)表达的晚期实体瘤成年患者的研究。
18.DS003冻干粉针
DS003冻干粉针是达石药业开发的一款生物创新药,拟开展治疗晚期恶性实体瘤的研究。
新药临床申请·新受理
本期,CDE新受理32新药(61个受理号)临床申请。其中,25个品种(49个受理号)为国产新药,7个品种(12个受理号)为进口新药,更多动态如下:
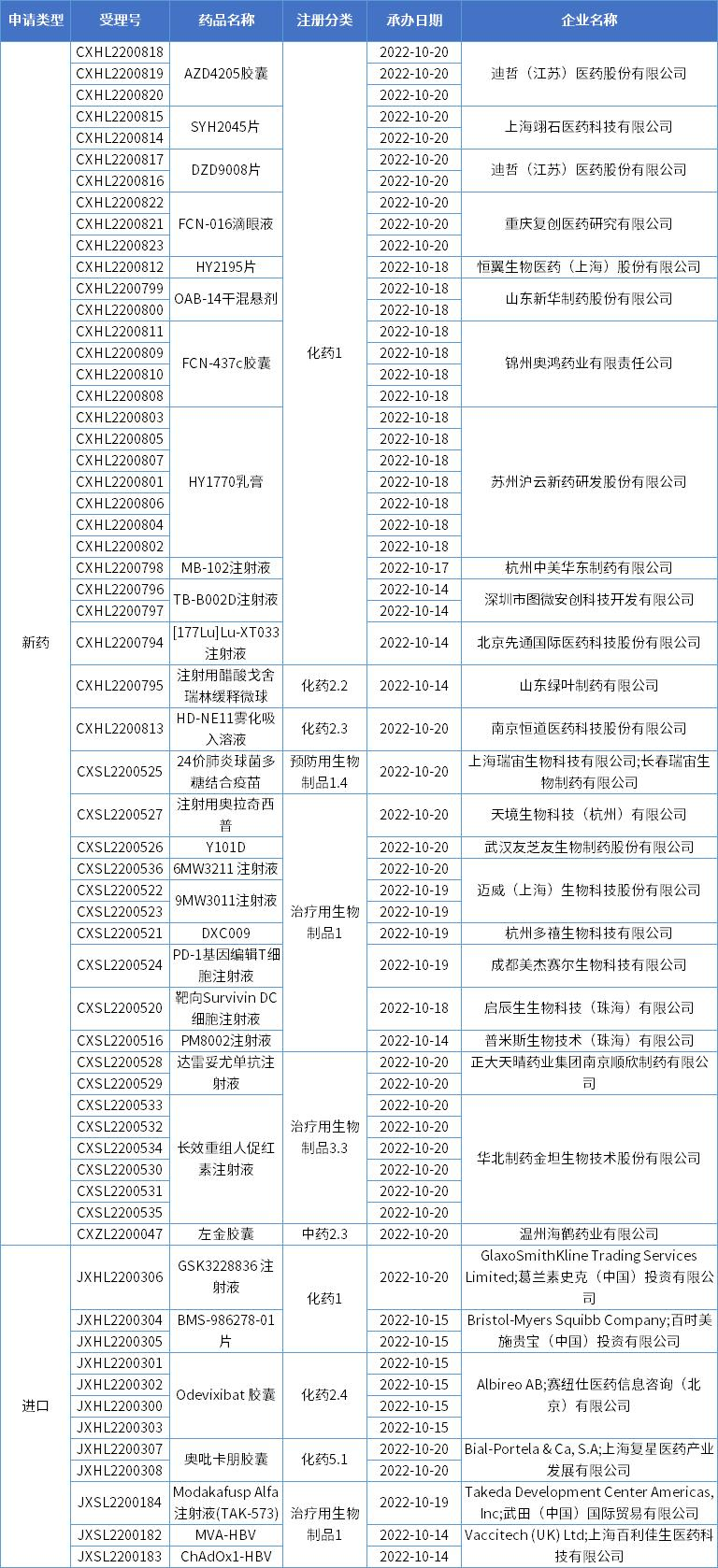
数据来源:药智数据、企业公告等网络公开数据
信息来源:药智网、企业公告等网络公开信息